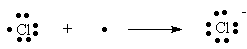terça-feira, 18 de novembro de 2008
segunda-feira, 17 de novembro de 2008
Grupo: Química do Futuro
Série:1º08
Elizabeth Mascarenhas
Clarice Couto
Carlos Manoel
Aristides Neto
Igor Gonçalves
Geismael dos Santos
Jéssica Janaína
Raysla Freire
Ícaro Cunha
Forças Intermoleculares
 todos parecem seguir uma regra de que quanto menor a massa molecular, menor é a temperatura de ebulição. Por esta regra (que parece ser obedecida na família do carbono), a água deveria ser, à temperatura ambiente, um gás, com uma temperatua de ebulição bem abaixo de 0 oC. Todos sabemos que, na verdade, a água é um líquido com ponto de ebulição de +100 oC!
todos parecem seguir uma regra de que quanto menor a massa molecular, menor é a temperatura de ebulição. Por esta regra (que parece ser obedecida na família do carbono), a água deveria ser, à temperatura ambiente, um gás, com uma temperatua de ebulição bem abaixo de 0 oC. Todos sabemos que, na verdade, a água é um líquido com ponto de ebulição de +100 oC!
A água, portanto, deve possuir um tipo de interação diferenciado. O que acontece é que os hidrogênios ligados ao oxigênio é que formam o lado "positivo" do dipolo permanente desta molécula. O átomo de hidrogênio é formado por apenas um próton e um elétron. Como o elétron é fortemente atraído pelo oxigênio, na água, este próton encontra-se desprotegido. A água possui, então, um dipolo bastante forte, com uma das cargas (positiva) bastante localizada. Este próton pode interagir com as regiões negativas (o oxigênio) de outras moléculas de água, resultando em uma forte rede de ligações intermoleculares. Esta interação é chamada de ligação
 hidrogênio, e ocorre entre átomos de hidrogênio ligados a elementos como o oxigênio, flúor ou nitrogênio, com átomos de O, N ou F de outras moléculas. Esta interação é a mais intensa de todas as forças intermoleculares.
hidrogênio, e ocorre entre átomos de hidrogênio ligados a elementos como o oxigênio, flúor ou nitrogênio, com átomos de O, N ou F de outras moléculas. Esta interação é a mais intensa de todas as forças intermoleculares.Como consequência das fortes interações intermoleculares, a água apresenta algumas propriedades especiais. Alguns insetos, por exemplo, podem andar sobre ela. Uma lâmina de barbear, se colocada horizontalmente, também flutua na água. Isto deve-se à tensão superficial da água: uma propriedade que faz com o líquido se comporte como se tivesse uma membrana elástica em sua superfície. Este fenômeno pode ser observado em quase todos os líquidos, e é o responsável pela forma esférica de gotas ou bolhas do líquido. A razão é que as moléculas de água interagem muito mais fortemente com suas vizinhas do que com as moléculas do ar, na interface. As moléculas que estão no interior da gota, por exemplo, interagem com outras moléculas em todas as direções; as moléculas da superfície, por outro lado, interagem somente com moléculas que estão nas suas laterais ou logo abaixo. Este desbalanço de forças intermoleculares faz com que estas moléculas, da superfície, sejam atraídas para o interior do líquido. Para se remover estas moléculas da superfície é necessário uma certa quantidade mínima de energia - a tensão superficial. Para a água, isto corresponde a 0,07275 joules/m2, a 20oC. Líquidos orgânicos, como o benzeno ou o tolueno, tem valores menores de tensão superficial, já que suas interações intermoleculares são mais fracas.
 pentano tenha uma temperatura de ebulição bem maior do que o neo-pentano? Observe que, à temperatura ambiente, o n-pentano é um líquido, enquanto que o outro isômero é um gás! Este caso ilustra uma propriedade das interações intermoleculares: quanto maior for a área de contato entre as moléculas, maior é a interação. No caso no neo-pentano, a interação é dificultada devido ao impedimento espacial provocado pelo grupos -CH3. A polarização induzida ocorre mais intensamente no caso da cadeia linear.
pentano tenha uma temperatura de ebulição bem maior do que o neo-pentano? Observe que, à temperatura ambiente, o n-pentano é um líquido, enquanto que o outro isômero é um gás! Este caso ilustra uma propriedade das interações intermoleculares: quanto maior for a área de contato entre as moléculas, maior é a interação. No caso no neo-pentano, a interação é dificultada devido ao impedimento espacial provocado pelo grupos -CH3. A polarização induzida ocorre mais intensamente no caso da cadeia linear. Uma outra propriedade pode ser observada se acompanharmos a temperatura de ebulição dos compostos ao lado. O éter dimetílico, embora possua a maior massa molar, é o que tem a menor Te (é um gás, à temperatura ambiente). Tanto o metanol como a água são líquidos, embora tenham massa molar menores. A água, a molécula mais leve da série, tem a maior temperatura de ebulição. Isto porque a água e o metanol interagem via ligação hidrogênio - a mais forte das interações intermoleculares, enquanto que o éter interage via dipolo-dipolo - não possue hidrogênios ligados ao oxigênio. A água possue dois hidrogênios ligados ao O - o que explica a sua maior temperatura de ebulição, em relação ao metanol, que possui apenas um. Como vemos, a substituição dos hidrogênios da água por grupos -CH3 leva a compostos com menor temperatura de ebulição.
Uma outra propriedade pode ser observada se acompanharmos a temperatura de ebulição dos compostos ao lado. O éter dimetílico, embora possua a maior massa molar, é o que tem a menor Te (é um gás, à temperatura ambiente). Tanto o metanol como a água são líquidos, embora tenham massa molar menores. A água, a molécula mais leve da série, tem a maior temperatura de ebulição. Isto porque a água e o metanol interagem via ligação hidrogênio - a mais forte das interações intermoleculares, enquanto que o éter interage via dipolo-dipolo - não possue hidrogênios ligados ao oxigênio. A água possue dois hidrogênios ligados ao O - o que explica a sua maior temperatura de ebulição, em relação ao metanol, que possui apenas um. Como vemos, a substituição dos hidrogênios da água por grupos -CH3 leva a compostos com menor temperatura de ebulição. açúcar é um exemplo: é muito solúvel em água. Isto deve-se à capacidade que as moléculas de água têm de interagir com as moléculas da sacarose. A solubilização também é um fenômeno regido pelas interações intermoleculares: entre as moléculas do soluto e as moléculas do solvente.
açúcar é um exemplo: é muito solúvel em água. Isto deve-se à capacidade que as moléculas de água têm de interagir com as moléculas da sacarose. A solubilização também é um fenômeno regido pelas interações intermoleculares: entre as moléculas do soluto e as moléculas do solvente.domingo, 16 de novembro de 2008
Polaridade das Moléculas
A eletronegatividade é definida simplesmente como "a tendência relativa de um átomo atrair para si o par de elétrons de ligação quando ligado a outro por uma ligação covalente". A definição parece um pouco longa, mas é fácil de se perceber o tremendo conteúdo que contém se fizermos uma análise bem simples das estruturas de Lewis e utilizarmos outro conceito básico que é a regra do octeto.
As estruturas de Lewis são assim: coloca-se o símbolo do elemento, e, em torno, pontinhos indicando o número de elétrons de valência do elemento. Portanto, elementos do grupo 1 da Tabela Periódica (tenha uma em mãos e mãos à obra) levam um pontinho (eles só possuem um elétron de valência):

Então vamos lá para a tal eletronegatividade: se o átomo tem a tendência de ganhar elétrons, ele vai por certo tentar também atrair para si o par de elétrons de ligação, quando engajado em uma ligação covalente. Veja como a noção pode se tornar intuitiva: como os halogênios (F, Cl, Br, I) só necessitam ganhar UM elétron para se tornarem parecidos com os seus gases nobres correspondentes, eles o farão com muita ansiedade, é muito fácil para eles conseguir esse último elétron, todos os halogênios são MUITO eletronegativos quando comparados com os outros elementos de seus respectivos períodos da Tabela Periódica. Já os calcogênios (geradores de cal, numa nomenclatura pré química) O, S, Se, Te necessitam de DOIS elétrons, e portanto têm um pouquinho mais dificuldade em conseguí-los, mas mesmo assim são tremendamente eletronegativos em relação aos outros átomos de seus respectivos períodos. Toda a família do nitrogênio N, P, As, Sb) necessita de três elétrons, e assim têm uma dificulidade maior ainda em obtê-los, portanto são menos eletronegativos, e assim sucessivamente. Assim funciona a família conhecida por NÃO METAIS. A família conhecida por METAIS é, por definição, eletropositiva, ou seja, "gostam" de perder elétrons ao invés de ganhá-los, pois assim fica fácil para eles atingirem a configuração eletrônica do gás nobre mais próximo, como no exemplo acima do elemento sódio transformando-se no cátion sódio.
Podemos então construir uma tabela de eletronegatividade para os elementos não metálicos do segundo período, incluindo aí o hidrogênio.
Onde não incluímos o berilo porque ele e todos os seus compostos são muito venenosos, e sua química não é portanto usual. Vamos ficar no mais trivial do nosso dia-a-dia.
Bom. É fácil compreender que os não metais vão formar compostos onde o compartilhamento de pares de elétrons de ligação é mais importante do que o perde - ganha que acontece entre metais e não metais quando eles se encontram. Isso porquê é energeticamente mais favorável para, digamos, o carbono compartilhar quatro elétrons com quatro hidrogênios diferentes, do que a alternativa de formar um íon C4- ladeado por quatro íons H+. Tal estrutura, C4-(H+)4 seria muito iônica, portanto teria as propriedades dos sólidos iônicos, como alto ponto de fusão, por exemplo, e no entanto, o CH4 é na verdade um gás (metano) à temperatura ambiente, o que indica que as suas ligações químicas tem de ter um quê de diferença. Esse quê é a ligação por compartilhamento de pares de elétrons, ou covalência.
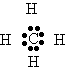
Segundo Lewis, a coisa ficaria assim:
Com os elétrons bem "pertinho" do carbono, porque ele é mais eletronegativo que o hidrogênio, e portanto tem maior tendência de atrair os pares de elétrons das ligações covalentes.
É fácil perceber que com a "aproximação" dos elétrons o carbono se torna POLARIZADO negativamente; por outro lado, cada hidrogênio "sente" a sua nuvem eletrônica cada vez mais longe, e por isso também se polariza, mas agora de uma forma positiva. Acabamos de formar um DI-polo, um polo positivo, e um negativo. Na linguagem da química, introduzimos a letra grega minúscula delta (d ) para mostrar cada polo do dipolo; no nosso caso, ficaríamos com quatro dipolos Cd-Hd+.
Agora vamos levar em consideração o formato da molécula de metano. Uma forma fácil de ver como funciona a coisa é a VSEPR (veja com detalhes em nossos Ensaios como a coisa funciona), que decreta que, com 4 conjuntos de elétrons ao seu redor, o carbono do metano tem de estar no centro de um tetraedro:
Onde o rabicho "+ " indica o lado positivo. No metano, os dipolos apontam para o carbono, dessa forma
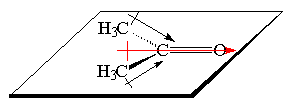
Um caso de uma molécula polar: a acetona. A geometria da acetona é trigonal plana, como conseqüência da hibridação sp2 do carbono central. A molécula, o plano, os dipolos e o dipolo resultante são esquematizados na figura abaixo.
Outro exemplo de uma molécula polar: o diclorometano, um solvente muito utilizado em laboratório, cuja fórmula é CH2Cl2, de estrutura tetraédrica. Os dipolos ficam assim:
Uma molécula polar da maior importância é a água, e é trivial ver como a somatória dos vetores polarização acabam em um dipolo permanente:
Uma advertência importante: as moléculas POLARES se atraem mais e melhor do que as APOLARES, pois um dipolo permanente implica na existência de uma área da molécula como d+ enquanto que em outra área o d é negativo. Ora, positivo atrai negativo e vice-versa, portanto, a acetona e o diclorometano discutidos acima são líquidos voláteis à temperatura ambiente, enquanto que os apolares gás carbônico e o metano, também discutidos acima, são gases: não existindo a força de atração molecular oferecida pela existência de um dipolo permanente, não há nada que atraia uma molécula à outra, e a tendência delas será a de ocupar o maior volume possível, que é a característica intrínseca de um gás.
Nesse contexto, a água é ainda excepcional, pois além da atração devido ao dipolo permanente, ela ainda indulge em ligações de hidrogênio --H-OH---H-OH--- o que a torna líquida até a estonteante temperatura de +100 ºC. Por comparação, o gás venenoso H2S (gás sulfídrico, o do cheiro do ovo podre) onde a baixa eletronegatividade do enxofre não permite a formação de pontes --H-SH---H-SH-- é mesmo um gás à temperatura ambiente, ainda que um fraco dipolo permanente exista na molécula.
Polaridade das Ligações
Ligação Covalente Polar: ocorre quando há diferença de eletronegatividade entre os átomos da ligação. Neste caso há a formação de um dipolo representado por um vetor m, orientado no sentido do átomo de menor eletronegatividade para o de maior, chamado momento de dipolo.
Exemplo:

Fonte:http://www.ficharionline.com/ExibeConteudo.php5?idconteudo=5904
Eletronegatividade
Assim, um átomo que, quando isolado, possui grande potencial de ionização e grande afinidade eletrônica também apresentará, quando ligado a outro átomo, grande atração por elétrons, ou seja, terá uma alta eletronegatividade.
Podemos dizer que a eletronegatividade depende de dois fatores: tamanho do átomo e número de elétrons na última camada. Já conhecemos a influência do primeiro desses fatores: quanto menor é o átomo, maior é sua capacidade de atrair elétrons, já que a distância destes ao núcleo é menor. O segundo fator se deve à tendência que os átomos possuem de se tornarem mais estáveis quando completam oito elétrons na última camada. Átomos com maior número de elétrons na última camada exercem maior atração sobre os elétrons de outros átomos.
É o balanço entre esses fatores que determina qual, dentre dois átomos, é o mais eletronegativo. Por exemplo, o cloro tem sete elétrons na última camada e o oxigênio, seis. Se fosse considerado apenas esse fator, o cloro seria mais eletronegativo que o oxigênio por precisar de apenas um elétron para completar o octeto. Entretanto, o átomo de oxigênio é tão menor que o de cloro que essa característica acaba por superar o outro fator. Como resultado, o oxigênio se revela mais eletronegativo que o cloro. Isso nos permite dizer que, de modo geral:
Quanto menor o átomo e maior o número de elétrons na última camada, maior é sua eletronegatividade.
Um gráfico da eletronegatividade em função do número atômico, seria:
A escala de eletronegatividade é uma escala arbitrária que representa a força do átomo para atrair elétrons. Ela se estende do césio, com eletronegatividade 0,7 até o flúor, com 4,0. A eletronegatividade não é um valor absoluto, mas sim relativo. Assim, a eletronegatividade de um elemento só é definida em termos de eletronegatividade de outros elementos. Diversas escalas foram sugeridas, incluindo as de R. S. Mullinken, L. Pauling e R.T. Sanderson. A escala de Pauling, a mais antiga, surgiu da consideração das energias necessárias para romper as ligações químicas nas moléculas. A eletronegatividade aumenta com a diminuição do tamanho atômico, tanto para elementos do mesmo período como para do mesmo grupo. Deve-se observar também que a eletronegatividade cresce com o aumento do número de elétrons de valência para os metais do Grupo I, II e III. Entre os aspectos úteis do conceito de eletronegatividade, está a oportunidade que ela nos proporciona para predizer certas propriedades químicas dos elementos. Podemos predizer o caráter de uma ligação química observando a diferença dos valores de eletronegatividades dos elementos:
quarta-feira, 12 de novembro de 2008
Geometria Molecular
Para se determinar a geometria de uma molécula, é preciso conhecer a teoria da repulsão dos pares eletrónicos da camada de valência.